2024年8月21日,中国科学院物理研究所姜道华团队在Nature在线发表题为”Human XPR1 structures reveal phosphate export mechanism“的研究论文,该研究展示了人类XPR1蛋白在Pi结合的封闭、开放和InsP6结合形式下的冷冻电镜结构,揭示了XPR1蛋白被InsPPs门控和调控的结构基础。

XPR1由N端SPX结构域、二聚体形成核结构域和Pi输运结构域组成。在输运域内,三个基本簇负责Pi结合和输运,一个保守的W573作为门控的分子开关。此外,SPX结构域与InsP6结合,通过释放限制Pi进入的C端环促进Pi外溢。该研究为了解真菌、植物和动物中XPR1同源物对Pi稳态的机制提供了一个概念框架。
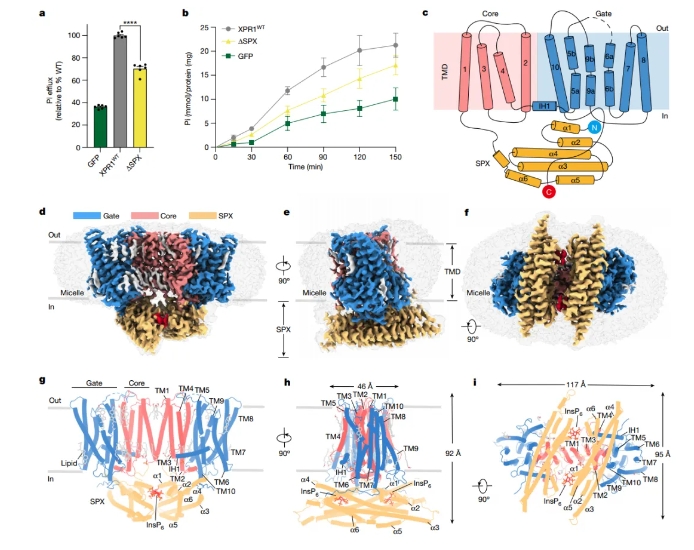
研究中,作者测定了人类XPR1蛋白结合Pi和己基磷酸肌醇(InsP6)在三种不同功能状态下的冷冻电镜(cryo-EM)结构,展示了XPR1样蛋白的结构特征和Pi输出机制。结合功能性诱变结果,该研究阐明了XPR1中Pi结合、门控、InsPP传感以及InsPP传感与Pi输出之间的耦合,这些对人类Pi稳态至关重要。